胡桃夹综合征(NCS),也称左肾静脉(LRV)压迫综合征,是一种泌尿外科里面较少见但是很重要的疾病。目前尚未有统一的诊断标准和管理办法。来自英国的 Ananthan 等专家整理前人的文献,并于 European Journal of Vascular and Endovascular Surgery 杂志上发表了一篇 NCS 相关指南。接下来,我们一起学习下这篇文章的重点。
1937 年,Grant 首次在解剖学上定义胡桃夹现象:LRV 夹在主动脉和肠系膜上动脉(SMA)之间,像胡桃夹的钳口间夹了一颗坚果。这种情况导致 LRV 在主动脉-肠系膜区域狭窄,血管远端部分扩张。1950 年,Sadr 和 Mina 首次描述主动脉和 SMA 对 LRV 的压迫。
然而,这种解剖并不总是导致临床症状。当胡桃夹现象引起血尿,蛋白尿和左腰腹痛等一系列临床症状时,称为 NCS(1972 年比利时放射科医师 De Scheper 命名)。
NCS 的确切流行率尚不清楚。因为诊断标准尚未统一,并且症状表现各式各样。NCS 可以出现在幼儿到七十岁的任何时间段,流行率在二三十岁和中年人中较高。
分类
NCS 有两种主要形式。最常见的是前 NCS,即 LRV 在腹主动脉和 SMA 之间受压。有人指出,在矢状面测量时,SMA 和腹主动脉之间的角度需要<45°,才能诊断 NCS;如果角度<35°,则足以进行明确诊断。Kim 等人指出, 角度<39°对于检测症状性 NCS 具有 92% 的敏感性和 89% 的特异性。
后 NCS 不太常见,表现为肾静脉在主动脉和脊柱椎体之间受压。另外据报道,由于重复 LRV 的存在,出现合并前部和后部 NCS 的情况。
临床症状
最常见的临床表现包括盆腔疼痛,腰痛,血尿和性腺静脉曲张(精索静脉曲张或卵巢静脉综合征),反射性盆腔和肾脏充血。NCS 的另一个常见症状是直立性蛋白尿。一些患者可以有严重的持续的症状,但一些患者(尤其是儿童)可能没有任何症状。
NCS 的诊断
NCS 的影像学检查包括多普勒超声(DUS),CT,MRI,静脉造影和血管内超声(IVUS)。然而,NCS 的诊断不能仅基于影像检查,临床症状和体征也尤为重要。具体诊断流程图见图 1。
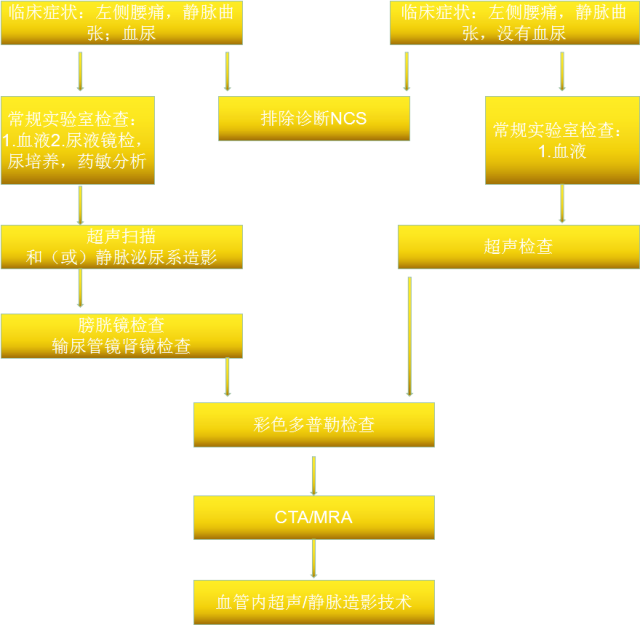
图 1 胡桃夹综合征诊断流程图
在诊断 NCS 方面,实时 DUS 有 69%~90% 的敏感性和 89%~100% 的特异性。DUS 被许多人推荐作为首选诊断性检查。但是因受体位因素等影响,它的指数和数值范围高度可变。
如果 DUS 无法诊断,需要轴向成像(CTA 和 MRA)。它们精确描述 LRV 和周围结构间的解剖情况,但是由于不是动态模式,不能精确测量血管流速和方向。
CT 最特别的发现是 LRV 直径比(肾门与主动脉-肠系膜处的比值)≥4.9,其特异度为 100 %。轴向 CT 中观察到的「鸟嘴征」是诊断准确性最高的。CT 有辐射暴露,并且存在造影剂过敏的可能。而 MRI 没有辐射,并且更好地描绘了软组织解剖情况。
如果诊断仍不清楚,可以通过静脉造影和测量 LRV 和下腔静脉之间的压力梯度,或者通过 IVUS 来确认。这两种侵入性方法都是诊断 NCS 的「金标准」。IVUS 有 90% 的特异性,而静脉造影的特异性为 62%。
Beinart 等人指出,在大多数健康人中,肾静脉和腔静脉平均压力梯度为 0~1 mmHg。如果静脉造影发现梯度>3 mmHg,则可以诊断 NCS。但是要注意,部分健康个体有>3 mmHg 的压力梯度,无症状患者的压力梯度范围可以很大。
治疗管理
NCS 的治疗仍然是一个有争议的话题。在轻度症状的情况下,建议保守治疗。
以下情况可以考虑手术:
严重血尿(尤其是复发性);
严重症状包括严重的(侧)腹部疼痛,贫血,自主功能障碍,肾功能损害(包括持续性直立蛋白尿,精索静脉曲张形成等);
对于<18 岁的患者,24 个月保守措施无效;
对于成年人,6 个月保守措施无效。
保守管理
18 岁或 18 岁以下的患者更倾向于保守治疗。随着年龄增长,SMA 来源的腹腔内和纤维组织增多,腹膜后脂肪组织增加,这些都可以缓解 LRV 受压情况。静脉侧支的发育也有助于缓解 LRV 的高压问题。药物治疗也已经开始使用,如血管紧张素转换酶抑制剂(特别是阿拉普利)用以改善直立性蛋白尿,阿司匹林用以改善肾脏灌注。
外科管理
开放手术:
1974 年,Pastershank 治疗了一例血尿合并左侧腰痛男性患者。手术主要是分离主动脉和 SMA 之间的纤维组织,游离受压的 LRV。这是第一份关于 NCS 外科治疗的报告。目前采用的开放手术包括 LRV 转位和自体肾移植。
LRV 转位需要切断下腔静脉连接处的血管,并于 SMA 远端重新连接。Stewart 和 Reiman 首次成功将静脉转位术应用于左肾,并报告了三个成功病例。目前认为,LRV 转位是治疗 NCS 的黄金标准,它也是这类患者最常用的外科治疗方法。手术是经腹腔进行的,所以有麻痹性肠梗阻,出血和血栓形成的风险。
自体肾移植是一种更具侵入性的手术,需要在左侧或右侧髂窝进行肾切除和肾移植。Hardy 等人首次报道了自体肾移植。有人指出,比起前者,自体肾移植在降低 LRV 压力方面更有效。然而这种手术有许多风险,包括增加肾缺血时间,需要更多手术暴露以及更多吻合术(肾动脉吻合和输尿管吻合)。
治疗 NCS 的另一种方法是 SMA 尾部的移位。这种方法需要术中暴露后腹膜,降低了肾静脉血栓形成的风险。然而,肠系膜缺血的风险很大。其他外科手术包括近端睾丸-髂-隐静脉吻合术(利用隐静脉连接睾丸静脉和髂静脉),性腺-腔静脉旁路术,盆腔周围静脉曲张切除术,肾-腔静脉旁路术,肾脏去包膜术和腔内球囊血管成形术等。
如果存在严重持续血尿情况,推荐肾切除术。
腹腔镜手术:
据文献报道,腹腔镜手术的结果与开放手术相近。主要包括腹腔镜脾肾静脉旁路术和腹腔镜 LRV-IVC 转位术。在腹腔镜脾肾静脉旁路术后 8 个月的随访中,Chung 等人发现患者的左侧疼痛有所改善。但是由于 LRV 排入门静脉系统,LRV 高压风险始终存在。另外还有因缺血和撕裂造成脾脏损害的风险。
许多其他腹腔镜手术已经开始应用。腹腔镜肠系膜下-性腺静脉旁路术避免了肾再灌注损伤和 LRV 高压的风险。与前面两种手术相比,它降低了脾切除的风险,也避开了胰腺位置的干扰。腹腔镜自体肾移植于 1995 年首次实施,应用普遍。这种微创手术有减少疼痛,缩短住院时间,改善切口外观和缩短康复期等优点。机器人辅助腹腔镜 LRV 转位术目前仅限于病例报告。
血管内支架植入术(EVS):
一项回顾性分析显示,在 6 个月的随访中,接受 EVS 治疗的大多数患者有一定程度的症状改善。66 个月的随访中,患者没有出现明显的再狭窄情况。此外,LRV 直径,峰值速度比和肾-腔静脉压力梯度都有所改善。
越来越多的数据证明 EVS 的可行性。有人认为,EVS 和开放手术一样可以作为首选治疗方式,EVS 可以优先用于治疗与盆腔充血相关的 NCS。它避免了复杂的吻合术,复杂的手术解剖和长时间肾缺血等问题。EVS 的风险包括支架放置出错需要手术干预,支架移动 (例如移动到右心房等),支架栓塞,支架内再狭窄,假内膜增生和血栓形成等。
值得注意的是,患者需要在支架植入后接受抗凝和抗血小板药物治疗。
