肾细胞癌是泌尿外科较为常见的肿瘤之一。其中,大约有 65% 为局限性肾癌,可通过外科手术方法根治;而 30% 的肾癌为转移性肾癌(mRCC),需要采用综合治疗方案。
随着近些年靶向药物的临床应用,转移性肾癌患者的生存期得到了明显提高。目前,共有 11 种药物被 FDA 批准用于转移性肾癌的一线及二线治疗(表 1)。转移性肾癌的治疗药物按照作用机理可分为三种:细胞因子,小分子激酶抑制剂以及免疫检查点抑制剂。
表 1. 转移性肾癌的一线/二线治疗药物一览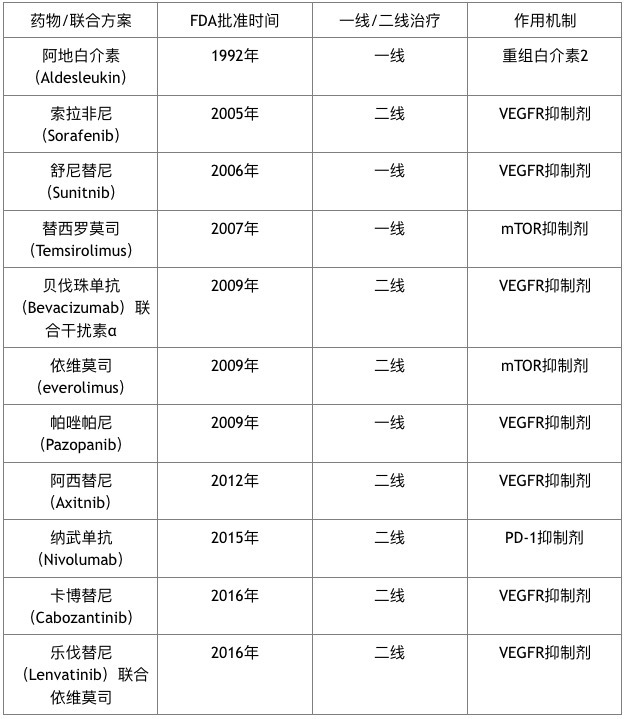
细胞因子
代表药物:阿地白介素(aldesleukin)
20 世纪 90 年代起,高剂量的白介素-2(IL-2)及其重组药物—阿地白介素,一直作为 mRCC 标准的一线治疗方案。然而,这类药物普遍的反应率只有 5%~27%,且对患者的长期存活改善不佳,加之副反应众多且严重,目前已逐渐被以下两种药物取代。
小分子激酶抑制剂
代表药物:索拉非尼(sorafenib),舒尼替尼(Sunitnib)
随着 2005 年第一款激酶抑制剂—索拉非尼被美国食品药物监管局(FDA)批准用于 mRCC 的化疗,靶向治疗逐渐进入大家的视野。此后,众多的新型多效激酶抑制剂/联合方案被 FDA 批准用于转移性肾癌的治疗,包括舒尼替尼(Sunitnib),替西罗莫司(Temsirolimus),贝伐珠单抗(Bevacizumab)联合干扰素α,依维莫司(everolimus),帕唑帕尼(Pazopanib),阿西替尼(Axitnib)。
2015 年后又有两种激酶抑制剂/联合方案被 FDA 批准:卡博替尼(Cabozantinib)和乐伐替尼(Lenvatinib)联合依维莫司。
激酶抑制剂可细分为血管表皮生长因子受体(VEGFR)抑制剂及 mTOR 受体抑制剂(表 1)。其中,VEGFR 抑制剂可通过抑制不同类型的 VEGFR(VEGFR-1,VEGFR-2,VEGFR-3)实现抑制肿瘤细胞增殖和转移的作用。
由于各类 VEGFR 抑制剂的受体不同,因此在一线 VEGFR 抑制剂,例如舒尼替尼和帕唑帕尼,治疗无效的情况下,某些二线 VEGFR 抑制剂仍可能发挥抑制作用,包括阿西替尼,卡博替尼和乐伐替尼(联合依维莫司)。
目前常用的 mTOR 抑制剂有两种,替西罗莫司和依维莫司。其中,替西罗莫司是一线化疗药物,而依维莫司需要联合 VEGFR 抑制剂用药。mTOR 抑制剂通过抑制肿瘤细胞中 mTOR 通路抑制肿瘤的进展,且不会与 VEGFR 抑制剂出现交叉耐药的现象,因此 mTOR 抑制剂可单独或与 VEGFR 抑制剂联合用药治疗 mRCC。mTOR 抑制剂的常见副反应包括肺炎和高钙血症。
相较于细胞因子治疗,患者对激酶抑制剂的反应性较高,且毒副作用较少,患者的中位生存期显著延长,因此现今转移性肾癌的药物治疗多以激酶抑制剂为主。
免疫检查点抑制剂
代表药物:纳武单抗(Nivolumab)
免疫检查点抑制剂可特异性抑制免疫细胞激活的免疫检查点,例如 CTLA-4 和 PD-1,从而阻止肿瘤细胞的免疫逃避。不同于激酶抑制剂,免疫检查点抑制剂的毒副作用相对较少,但有导致自体免疫毒性,对内分泌、胃肠道、呼吸等系统产生影响。
纳武单抗是第一个也是唯一被 FDA 批准用于 mRCC 化疗方案的免疫检查点抑制剂。纳武单抗是抗 PD-1 抗体,可特异性抑制 PD-1,从而通过抑制 T 细胞的功能促进自体免疫耐受。研究表明,在接受一种或者两种 VEGFR 抑制剂后使用纳武单抗的患者中位生存期显著提升,副反应显著降低。
目前,众多免疫检查点抑制剂仍处于临床试验阶段,包括抗 PD-1 抗体,派姆单抗(pembrolizumab);抗 PD-L1 抗体,阿特珠单抗(atezolizumab)和巴文西亚(Bavencio;avelumab);抗 CTLA-4 抗体,易普利姆玛(ipilimumab)。
展望
服用不同类型的激酶抑制剂可导致患者出现相应的并发症,长期服用还可能出现耐药性,因此药物联合治疗 mRCC 成为进一步提高治疗反应率、降低副反应的方法。
目前常用的方案为乐伐替尼联用依维莫司,临床试验表明,接受该方案的患者中位生存期得到了显著提升;相比单独用药,该方案的毒性较多,但仍处于可控状态。该方案已于 2016 年被 FDA 批准用于 mRCC 的药物治疗。目前处于临床试验阶段的联合方案还包括:依维莫司联用贝伐珠单抗,TRC105(抗内皮因子/CD105 抗体)联用阿西替尼或贝伐珠单抗等。
参考文献:
1. Posadas EM, Limvorasak S, Figlin RA. Targeted therapies for renal cell carcinoma. Nature reviews Nephrology. 2017;13(8):496-511.
2. Motzer RJ, Hutson TE, Glen H, Michaelson MD, Molina A, Eisen T, et al. Lenvatinib, everolimus, and the combination in patients with metastatic renal cell carcinoma: a randomised, phase 2, open-label, multicentre trial. Lancet Oncol. 2015;16(15):1473-82.
3. Rosen LS, Hurwitz HI, Wong MK, Goldman J, Mendelson DS, Figg WD, et al. A phase I first-in-human study of TRC105 (Anti-Endoglin Antibody) in patients with advanced cancer. Clin Cancer Res. 2012;18(17):4820-9.
4. Rosen LS, Gordon MS, Robert F, Matei DE. Endoglin for targeted cancer treatment. Curr Oncol Rep. 2014;16(2):365.
5. Tomita Y, Fukasawa S, Shinohara N, Kitamura H, Oya M, Eto M, et al. Nivolumab versus everolimus in advanced renal cell carcinoma: Japanese subgroup analysis from the CheckMate 025 study. Japanese journal of clinical oncology. 2017:1-8.
